近日,基础医学院初波教授课题组的最新研究成果“Peroxisome-driven ether-linked phospholipids biosynthesis is essential for ferroptosis”在Cell Death & Differentiation上在线发表(中科院JCR期刊1区,最新IF:10.717,五年IF:9.597)。太阳集团8722c基础医学院细胞生物学系初波教授和哥伦比亚大学顾伟教授为该论文的共同通讯作者,太阳集团8722c基础医学院博士研究生崔伟伟为该论文的第一作者,太阳集团8722c为唯一通讯单位。
铁死亡(Ferroptosis)是2012年由Brent R. Stockwell实验室首次发现并提出的一种新型的细胞死亡方式,它是铁离子依赖的脂质过氧化物过度累积所致,其在形态、生物学特征和机制调控区别于细胞凋亡、坏死、自噬及焦亡。近年来,铁死亡在肿瘤发展、神经退行性疾病、缺血再灌注损伤、炎症反应等病理过程中的作用受到广泛关注。脂质代谢在铁死亡发生过程中发挥着重要作用,以往研究一直认为只有多不饱和脂肪酸能够促进细胞铁死亡的发生,而本论文首次发现饱和脂肪酸可通过脂肪醇-醚酯途径促进细胞铁死亡的发生。
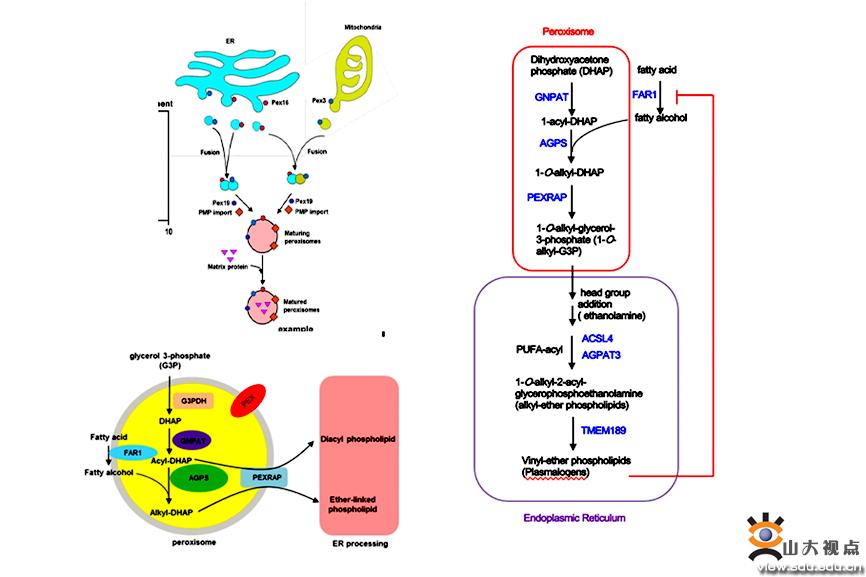
为深入探究人体内源代谢物是如何调控铁死亡发生的,作者对近400种内源性小分子代谢物进行筛选,发现了多种能够促进或保护细胞铁死亡的化合物,其中发现16碳饱和脂肪醇1-hexadecanol (1-HE)可显著促进肿瘤细胞发生铁死亡。1-HE属于饱和脂肪醇,由饱和脂肪酸棕榈酸还原而成,此过程是由过氧化物酶酶体脂肪酰基辅酶a还原酶FAR1催化完成,饱和脂肪醇后在AGPS和GNPAT等醚酯合成相关酶的作用下,合成醚酯。通过Genome-wide CRISPR-CAS9 Screening 和生物信息学等技术分析发现,过氧化物酶体途径参与醚酯的生物合成,而这一过程也被证实是1-HE和FAR1发挥促细胞铁死亡作用所必需的。TMEM189,能够引入乙烯基醚双键到烷基醚脂质中产生缩醛磷脂(醚酯的一种),可取代FAR1 -烷基醚脂质轴诱导铁死亡的作用,这提示TMEM189有望成为抗癌治疗的药物靶点。
初波教授团队致力于铁死亡与代谢、肿瘤及神经退行性疾病的研究,深入探究肿瘤发展过程中铁死亡的作用及其机制,取得了一系列原创性成果,先后发表在顶级期刊Nature Cell Biology,Molecular Cell,PNAS & Nature Communication,总引用率319次,很好地推动了铁死亡领域的研究进展。
文章链接:https://doi.org/10.1038/s41418-021-00769-0